Антиноцицептивный эффект хондропротекторов
Антиноцицептивный эффект хондропротекторов — миф или реальность?
А.Б.Данилов
доктор медицинских наук, профессор кафедры нервных болезней ИПО Первого МГМУ им. И.М. Сеченова,
председатель Совета экспертов Ассоциации междисциплинарной медицины.
Несмотря на то что у подавляющего большинства взрослых лиц в возрасте старше 30 лет выявляют различные формы структурной дегенерации одного или более дисков, это не всегда сопровождается болями и может быть проявлением процесса старения. Показано, что грыжи межпозвонковых дисков часто не сопровождаются болевым симптомом [1, 2].
РОЛЬ ПРОВОСПАЛИТЕЛЬНЫХ ЦИТОКИНОВ ПРИ БОЛЯХ, СВЯЗАННЫХ С ДЕГЕНЕРАЦИЕЙ ДИСКА
Дегенерация диска опосредована нарушением образования провоспалительных медиаторов, секретируемых клетками пульпозного ядра, фиброзного кольца, макрофагами, Т-лимфоцитами и нейтрофилами.
Эти цитокины запускают каскад патофизио- логических реакций со стороны клеток межпозвонковых дисков, которые могут стимулировать ускоренное старение и апоптоз [3–5].
Процесс дегенерации межпозвонкового диска характеризуется подъемом уровней провоспалительных цитокинов: ФНО-a, ИЛ-1a/b, ИЛ-6, ИЛ-17, ИЛ-8, ИЛ-2, ИЛ-4,ИЛ-10, хемокинов, простагландинов.
Среди провоспалительных цитокинов наиболее изученными являются ФНО-a и ИЛ-1b [6]. ФНО-a участвует в процессах образования грыжи диска, раздражения нервов и врастания сосудов [7], в то же время ФНО-a и ИЛ-1b способствуют повышению активности генов, кодирующих ферменты, участвующие в разрушении матрикса [8].
Такие же провоспалительные цитокины синтезируют «стареющий» межпозвонковый диск. Реактивные изменения клеток межпозвонкового диска сопровождаются секрецией провоспалительных цитокинов, хемокинов, матриксных протеаз. Данный феномен получил название SASP (SEN- SCENCE ASSOCIATED SECRETORY PHENOTYPE).
В результате дисбаланс катаболических и анаболических процессов приводит к дегенеративным изменениям, развитию протрузии и возникновению дискогенной и радикулярной боли. Миграция иммуноцитов в структуре диска сопровождается разрастанием мелких сосудов и нервных волокон, происходящих из ганглионарных клеток задних корешков.
В этой воспалительной среде выделение таких нейрогенных субстанций, как фактор роста нервов и мозговой нейротрофический фактор, генерируемых структурами межпозвонкового диска и иммунными клетками, вызывает активацию катионных каналов спинномозгового ганглия. Деполяризация этих каналов может инициировать дискогенную и радикулярную боль и усиливать регулируемый цитокинами дегенеративный каскад [9, 10].
В исследовании D. Kraychete и соавт. продемонстрировано, что у лиц с грыжей межпозвонкового диска наблюдается повышение уровней ФНО-a и ИЛ-6 в плазме в сравнении со здоровыми [11].
Пред- полагается, что повышение экспрессии цитокинов может участвовать в процессах, способных модифицировать факторы транскрипции, вовлеченные в генную экспрессию, вызывая экспансию глиальных клеток и, таким образом, приводя к повышению нейрональной гипервозбудимости.
Увеличение концентрации цитокинов в тканях области протрузии диска позволяет предположить их возможную роль в воз- никновении эндоневрального отека и демиелинизации нервных волокон. Кроме того, возбуждая ноцицепторы, цитокины играют ведущую роль в периферической гипералгезии и формировании болевого ответа [12].
В различных исследованиях неоднократно показано, что клетки межпозвонкового диска могут продуцировать ФНО-a и ИЛ-1b уже на начальных этапах протрузии диска [13, 14].
A. Koch и соавт. наблюдали, что увеличение плазменных уровней провоспалительных цитокинов (ИЛ-1, ИЛ-2, ИЛ-6 и ФНО-a) коррелирует с усилением интенсивности бо- ли у пациентов с хронической болью [15].
В многочисленных клинических исследованиях показано, что на фоне терапии дегенеративных заболеваний позвоночника хондропротекторами отмечается как выраженный симптом-модифицирующий эффект (уменьшение тугоподвижности, болевого синдрома), так и структурно-модифицирующий эффект (восстановление трофики тканей хряща и сустава, улучшение рентгенологической картины). Одним из действующих веществ с доказанным антиноцицептивным эффектом при лечении боли в спине является хондроитина сульфат.
ХОНДРОИТИНА СУЛЬФАТ
Хондроитина сульфат (ХС) представляет собой гетерогенный класс полисахаридов, что обусловлено наличием разного числа сульфатных групп, присо- единяющихся в различных позициях, и различиями в молекулярном весе (мол. масса 20000–30000).
Антиноцицептивный эффект хондропротекторов — миф или реальность?
ХС — гликозаминогликан (ГАГ), представленный в некоторых тканях тела, ингибирует разрушение хряща.
Важнейшим классом ферментов, разрушающих ткань хряща, являются матриксные металлопротеиназы (ММП).
Показано, что ХС на 28 % ингибирует синтез ММП-3 (ключевое звено гомеостаза суставных протеогликанов) хондроцитами, индуцированный ИЛ-1b [16].
В модели ОА у крыс ХС предотвращал повышение уровня ММП-9 — пускового момента хрящевой и костной деградации [17].
Было продемонстрировано, что ХС снижает активность индуцированной липополисахаридами ММП-13 в хондроцитах, что сопровождается уменьшением активации р38митоген-активированной белковой киназы и экстрацеллюлярной сигнальной регулирующей киназы [18].
В другом исследовании ХС уменьшал ИЛ-1b индуцированную экспрессию ММП-13 хондроцитами [19].
Позднее было установлено, что ХС, зависимым от дозы образом, на модели остеоартрита у кроликов подавляет стимулированный ИЛ-1 синтез простагландина синовиальными фибробластами, отменяет зависимую от ИЛ-1 ингибицию синтеза гиалуроновой кислоты, ингибирует (в отличие от глюкозамина) зависимый от ИЛ-1 синтез коллагеназы и активность аггреканазы (фермента, участвующего в разрушении протеогликана хряща) [20].
В исследовании in vitro ХС подавлял индуцированную ИЛ-1b экспрессию ЦОГ-2 и простагландин (ПГЕ) [21]
Повышение провоспалительных цитокинов в межпозвонковом диске приводит к снижению синтеза ХС, причем степень снижения содержания ХС в диске прямо пропорцианальна степени его дегенерации.
В настоящее время в терапии дегенеративно- дистрофических заболеваний суставов и позвоночника используют различные лекарственные формы ХС. Широкое применение нашли препараты, представляющие собой раствор ХС для внутримышечного применения. Преимуществом внутримышечного введения препарата ХС является быстрое всасывание в системный кровоток с на- коплением в синовиальной жидкости через 15 ми- нут, а в хрящевой ткани — через 30 минут.
Максимальная концентрация ХС в суставном хряще при его внутримышечном введении достигается через 48 часов [22].
Кроме того, внутримышечный способ введения ХС увеличивает биодоступность и долю нативных молекул в системном кровотоке, что приводит к повышению эффективности проводимой терапии и более быстрому развитию симптоматического эффекта [23].
Первый лекарственный препарат фармацевтической субстанции ХС в форме раствора для инъекций был синтезирован и апробирован в 1987 г. во Всесоюзном научно-исследовательском институте технологии кровезаменителей и гормональных пре- паратов (ВНИИТКГП).
Под руководством заведующей лабораторией биоконтроля гормонов и органопрепаратов д.м.н. Белай В.Б. было проведено экс- периментальное изучение специфического фармакологического действия препарата ХС, условно названного «Артрон», затем получившего название«Мукосат».
В дальнейшем оригинальный ХС — лекарственный препарат Мукосат® — прошел все фазы регистрационных исследований и с 1994 г. используется в качестве лекарственного средства у взрослых для лечения дегенеративно-дистрофичеcких заболеваний с доказанными симптом- и струrтурно-модифицирующими эффектами (рис. 1).
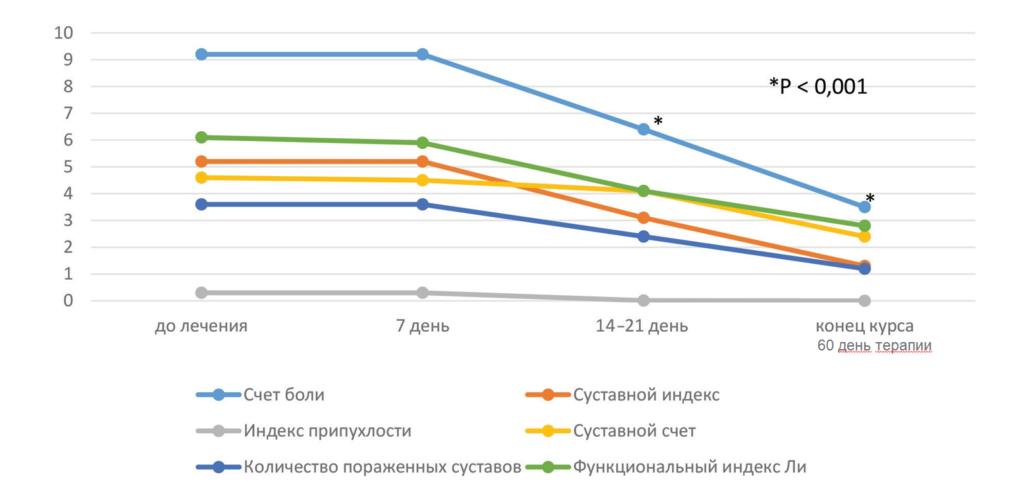
Рис. 1. Динамика суставного синдрома (интегральная оценка) при применении парентеральной формы хондроитина сульфата (Мукосат®) [24]
В отличие от биоактивных концентратов, Мукосат® имеет изученную фармакокинетику: через 15 минут после внутримышечной инъекции ХС обнаруживается в синовиальной жидкости, затем он попадает в суставной хрящ, где его содержание достигает мак- симума через 48 часов [25].
ХОНДРОИТИНА СУЛЬФАТ В КОКРАНОВСКОМ СИСТЕМАТИЧЕСКОМ ОБЗОРЕ
В 2015 г. были опубликованы результаты оценки эффекта хондроитина в купировании болевого синдрома [26].
43 исследования с участием 9110 пациентов были отобраны из числа найденных в электронных ресурсах публикаций и включены в обзор. В рамках 43 исследований 4962 пациента получали терапию хондроитином (в монотерапии или в комбинации с глюкозамином, НПВП), 4148 участников были включены в группы контроля.
Длительность исследований составляла от одного месяца до трех лет. Данные для метаанализа были собраны из 30 исследований, остальные исследования не были включены в метаанализ по причине расхождения основных критериев оценки, использованных в метаанализе.
Из 30 исследований в 18 оценивалась эффективность ХС по сравнению с плацебо, в 3 сравнивался хондроитин с контролем, в 7 — комбиниро- ванная терапия хондроитином и глюкозамином с плацебо, в 8 изучалась комбинированная терапия хондроитином и глюкозамином по сравнению с контролем.
ХОНДРОИТИНА СУЛЬФАТ В СРАВНЕНИИ С ПЛАЦЕБО: ВЛИЯНИЕ НА БОЛЬ
В 12 исследованиях оценивалась динамика болевого синдрома на фоне приема хондроитина или плацебо [26].
По результатам исследований длительностью до 6 месяцев, подтвердилось статистически достоверное преимущество активной терапии: у пациентов, которые принимали ХС, оценки выраженности боли по визуальной аналоговой шкале (ВАШ) от 0 до 100 мм были в среднем на 10,1 мм меньше, чем в группах плацебо. Клинически значимым считается уменьшение оценки боли на 0,9–1,3 см по шкале 0–10 см [A.M. Kelly, 1998; A.M. Kelly, 2001; K.H. Todd, 1996].
Результаты анализа влияния на боль: монотерапия хондроитином или в комбинации с глюкозамином обеспечивает клинически значимое и статистически достоверное облегчение боли по сравнению с плацебо. Абсолютный эффект улучшения составил 9–10 % и соответствует клинически значимому порогу.
В in vitro исследовании была продемонстрирована способность биоактивного концентрата, содержащего ХС, на 16 % снижать внеклеточное высвобождение ИЛ-6 в культуре хондроцитов [37].
Кроме того, на 35 % снижалось высвобождение ИЛ-8, который является хемокином, устанавливающим хемотаксический поток к суставной поверхности и усиливающим воспалительный процесс за счет присоединения лимфоцитов и нейтрафилов.
Другие авторы выявили, что под влиянием биоактивного концентрата, содержащего ХС, присходит снижение высвобождения фактора роста эндотелия сосудов (VEGF) на 56 % [38].
Интерпретируя данное наблюдение на клиническую практику, автор делает предположение, что за счет меньшего высвобождения VEGF происходит снижение неоангиогенеза и уменьшение аутокринной стимуляции хондроцитов, что должно оказывать положительные иммунопатогенетические эффекты [37].
ХОНДРОИТИНА СУЛЬФАТ В СРАВНЕНИИ С ПЛАЦЕБО: БЕЗОПАСНОСТЬ И ПЕРЕНОСИМОСТЬ
В 15 исследованиях получены данные общей частоты отмены препаратов. Количество участников, которым терапию пришлось отменить по любым причинам, не различалось достоверно между группами хондроитина и плацебо [26].
В 10 исследованиях —4 краткосрочных (до 6 месяцев наблюдения) и 6 долгосрочных (более 6 месяцев наблюдения) — получены данные о частоте отмены препаратов по причине развития побочных эффектов.
Статистически достоверных различий между группами хондроитина и плацебо не отмечено. В 8 исследованиях регистрировали частоту побочных эффектов. Статистически достоверных различий между группами хондроитина и плацебо не выявлено. В 6 исследованиях регистрировали частоту серьезных побочных эффектов. По данным долгосрочных наблюдений, риск был достоверно меньшим в группе хондроитина по сравнению с группой плацебо.
Согласно данным краткосрочных исследований, достоверных различий не было.
В 2017 г. в Росздравнадзор был подан «Периодический отчет по безопасности применения лекарственного препарата «Мукосат®» за отчетный период 27 июля 2015 г. — 30 мая 2017 г., в котором на основании зафиксированной за этот период только одной нежелательной реакции сделан вывод, что опыт пострегистрационного применения лекарственного препарата Мукосат® (раствор для внутримышечного введения) свидетельствует о стабильно положительном соотношении «польза — риск» [27].
ХОНДРОПРОТЕКТОРЫ В ЛЕЧЕНИИ ХРОНИЧЕСКОГО БОЛЕВОГО СИНДРОМА
Заслуживают интерес результаты проспективного экспериментального пилотного клинического исследования Robert G. Klein и соавт. [39], в котором приняли участие 36 пациентов в возрасте от 27 до 62 лет, страдающих длительной (около 8 лет) хроничес- кой болью в спине, не поддающейся консервативному и физиотерапевтическому лечению.
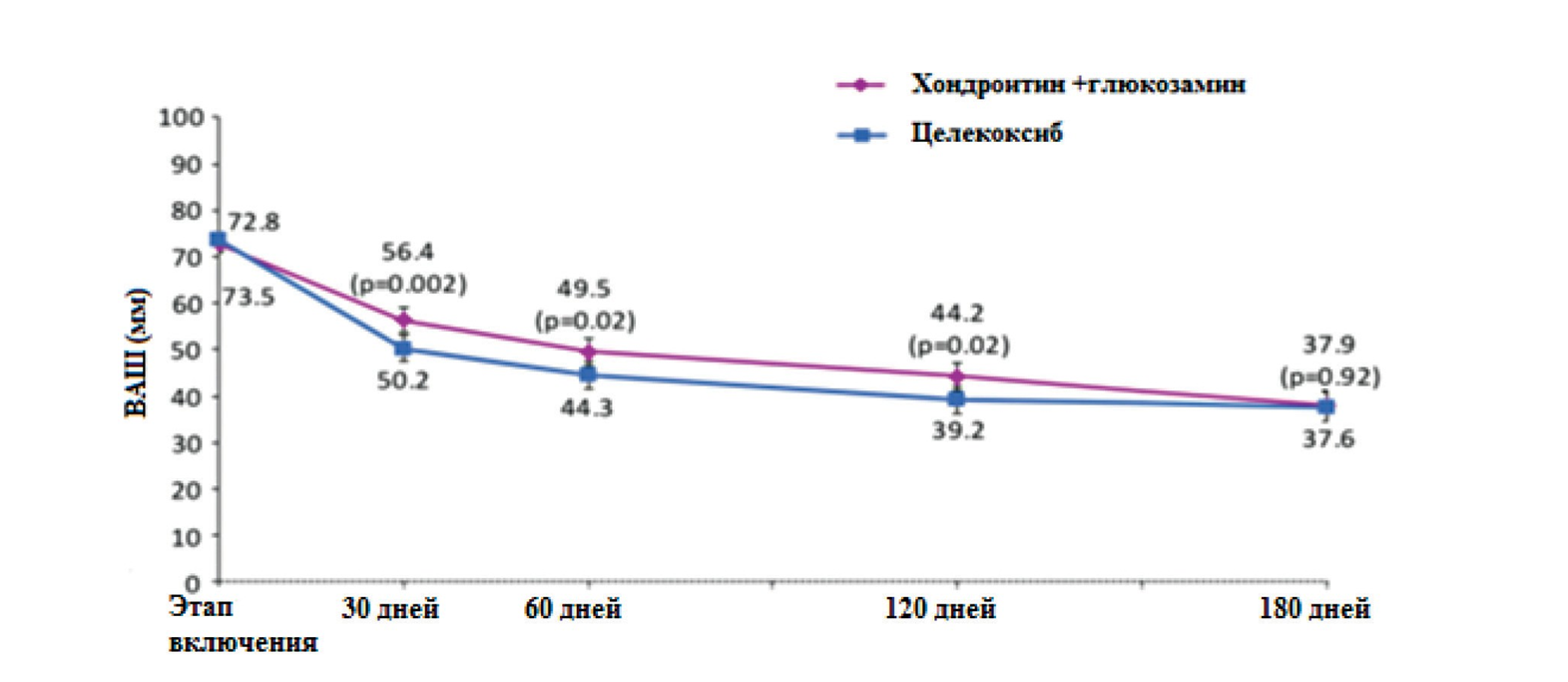
Рис. 2. Динамика болевого синдрома (по ВАШ) на фоне терапии глюкозамином и хондроитином (фиолетовым) и целекоксибом (синий) в течение 6 месяцев. Примечательно, что у целекоксиба в первые недели эффект более выраженный, а впоследствии перестает нарастать, в то время как в группе хондропротекторов отмечается умеренное плавное развитие антиноцицептивного эффекта, неуклонно нарастающего со временем.
Проводились внутридисковые инъекции 1–2 мл раствора, содержащего ХС, глюкозамин, диметилсульфоксид, маркаин и декстрозу. Аналогичные инъекции, но без ХС, проводились в дугоотросчатые суставы на уровне пораженного диска.
Количество манипуляций — от 1 до 4. По результатам терапии у 17 из 30 пациентов отмечалось снижение болевого синдрома по ВАШ на 76 %, а улучшение качества жизни — на 72 % по сравнению с исходным уровнем. У 13 пациентов, напротив, отмечался минимальный ответ на предложенную терапию со средними улучшениями показателей ВАШ на 14 % и улучшения качества жизни на 8 %.
АНТИНОЦИЦЕПТИВНЫЙ ЭФФЕКТ ХОНДРОПРОТЕКТОРОВ В СРАВНЕНИИ C ЦЕЛЕКОКСИБОМ
В двойном слепом мультицентровом клиническом исследовании хондропротекторы продемонстрировали антиноцицептивный эффект, сопоставимый с аналогичным эффектом селективных ингибиторов ЦОГ-2 (циклооксигеназа-2) [28].
В исследовании принимали участие 606 пациентов старше 40 лет с коленным остеоартритом, подтвержденным рентгенологически, и выраженным болевым синдромом (> 301 болевого индекса WOMAC по шкале от 0–500), рандомизированных в две группы.
Пациенты первой группы получали комбинацию ХС 400 мг и глюкозамина гидрохлорида 500 мг ежедневно, 3 раза в день, в течение 6 месяцев.
Пациенты второй группы получали целекоксиб 200 мг и плацебо в первый прием и по две капсулы плацебо в остальные два приема. Результаты показали, что терапия комбинацией хондропротекторов по своим противоболевым эффектам сопоставима с целекоксибом.
В течение 6 месяцев отмечалось уменьшение боли по ВАШ на 48,0 % в группе хондропротекторов по сравнению с 48,8 % в группе целекоксиба (рис. 2).
ЗАКЛЮЧЕНИЕ
Наряду с дегенеративными изменениями в развитии и прогрессировании остеоартроза весьма важную роль играет воспаление. В пораженном суставе усиливается продукция провоспалительных цитокинов, циклооксигеназы, что инициирует реакции воспаления и усугубляет повреждение хрящевой ткани и окружающих сустав структур.
Ключевое значение в каскаде провоспалительных медиаторов отводится ИЛ-1b, который экспрессируется в пораженном остеоартрозом хряще и стимулирует выработку металлопротеиназ [34]. Кроме того, ИЛ-1b тормозит экспрессию коллагена и протеогликанов, стимулирует синтез и высвобождение эйкозаноидов — простагландинов и лейкотриенов.
Традиционно хондропротекторы рассматривались исключительно как вещества, влияющие лишь на трофику хряща и его структуру, и их эффекты зачастую связывали с непосредственным влиянием на хрящевую ткань и ее частичным восстановлением.
Однако в многочисленных клинических исследованиях было продемонстрировано, что симптом-модифицирующий эффект (а именно уменьшение болевого синдрома) наступает гораздо раньше, чем восстанавливается структура хрящевой ткани.
Результаты ряда рандомизированных плацебо- контролируемых исследований демонстрируют выраженный антиноцицептивный эффект хондропротекторов, сравнимый с НПВП, не только в терапии остеоартроза, но и при хронической боли в спине, что открывает перед клиницистами новые возможности в лечении этого состояния. Следует помнить, что побочные эффекты при дли- тельном приеме НПВП гораздо более часты и опасны, чем таковые у хондропротекторов [35, 36].
Назначение комбинации НПВП и хондропротектора с первых дней лечения позволяет снизить потребность в НПВП, замедляет дальнейшее развитие заболевания.
Понимание закономерностей и связей между использованием хондропротекторов и биомаркерами воспаления может пролить свет на вовлеченные в процесс биологические механизмы. Антиноцицептивный эффект хондропротекторов, вероятно, связан с непосредственным влиянием на провоспалительные цитокины, маркеры системного воспаления. Как было показано in vitro и in vivo, ХС блокирует эффекты ИЛ-1b.
У пациентов, применявших высокие дозы ХС, наблюдалось снижение высокочувствительного СРБ в крови и снижение PGE-M в моче.
На сегодняшний день представления о механизмах действия так называемых «хондропротекторов» существенно изменились. Это связано прежде всего с открытием их независимых противовоспалительных и анальгетических свойств. Полученные в многочисленных исследованиях данные, подтверждающие способность этих препаратов ингибировать провоспалительные цитокины, открывают новые перспективы их применения в терапии не только артралгий, но и других хронических болевых синдромов.
Рассмотренные выше результаты достоверно подтверждают наличие антиноцицептивного эффекта у хондропротекторов, который характеризуется ранним началом и постепенным развитием с длительным сохранением результата даже после отмены терапии. В настоящее время эффективность хондропротекторов изучена и подтверждена во многих экспериментальных и клинических исследованиях [29–32].
Они являются обязательным компонентом комплексной терапии остеоартроза, рекомендованы с этой целью Европейской антиревматической лигой (EULAR) для уменьшения боли, улучшения функции суставов; эффект сохраняется в течение нескольких месяцев после их отмены, кроме того, они хорошо переносятся больными [33].
Применение хондропротекторов замедляет прогрессирование дегенеративных изменений суставов и позвоночника, оказывает отсроченное противовоспалительное и обезболивающее действие.
С учетом вышеизложенного при подборе комплексного лечения дорсалгий важно включение в комплексную терапию лекарственных препаратов, патогенетическое действие которых проявляется как улучшением состояния межпозвонковых дисков и фасеточных суставов, так и уменьшением выраженности воспалительных процессов в перечисленных структурах.
Безусловно, необходимы новые исследования для уточнения важных для клиницистов вопросов дозировок, сроков и предикторов лечения, оценки возможных нежелательных эффектов при разных типах болевых синдромов.
Литература
- 1. Cheung KM, Karppinen J, Chan D, Ho DW, Song YQ, Sham P, Cheah KS, Leong JC, LukKD. Prevalence and pattern of lumbar magnetic resonance imaging changes in a population study of one thousand forty-three individuals // Spine (Phila Pa 1976). 2009 Apr 20; 34 (9): 934–40.
- 2. Kanayama M, Togawa D, Takahashi C, Terai T, Hashimoto T. Cross-sectional magnetic resonance imaging study of lumbar disc degeneration in 200 healthy individuals // J Neurosurg Spine. 2009 Oct; 11 (4): 501–7.
- 3. Roberts, Sally PhD; Evans, Helena BSc; Trivedi, Jayesh MCh (Orth), FRCS, FRCS (Tr&Orth); Menage, Janis HND. Histology and Pathology of the Human Intervertebral Disc // Journal of Bone & Joint Surgery — American Volume. 88 (suppl_2) Supplement 2: 10–14, April 2006.
- 4. Purmessur D1, Walter BA, Roughley PJ, Laudier DM, Hecht AC, Iatridis J. A role for TNF-a in intervertebral disc degeneration: a non-recoverable catabolic shift // Biochem Biophys Res Commun. 2013 Mar 29; 433 (1): 151–6.
- 5. Chao Shen, Jun Yan, Lei-Sheng Jiang, and Li-Yang Dai. Autophagy in rat annulus fibrosus cells: evidence and possible implications // Arthritis Res Ther. 2011; 13 (4): R132. Published online 2011 Aug 16.
- 6. Shamji MF, Setton LA, Jarvis W, So S, Chen J, Jing L, Bullock R, Isaacs RE, Brown C, Richardson WJ. Proinflammatory cytokine expression profile in degenerated and herniated human intervertebral disc tissues // Arthritis Rheum. 2010; 62: 1974– 82.
- 7. Hayashi S., Taira A., Inoue G., Koshi T., Ito T., Yamashita M., Yamauchi K., Suzuki M., Takahashi K., Ohtori S. TNF-alpha in nucleus pulposus induces sensory nerve growth: a study of the mechanism of discogenic low back pain using TNF-alpha-deficient mice
// Spine (Phila Pa 1976). 2008 Jun 15; 33 (14): 1542–6. - 8. Le MaitreCL, Freemont AJ, Hoyland JA. The role of interleukin–1 in the pathogenesis of human intervertebral disc degeneration // Arthritis Res Ther. 2005; 7 (4): R732–45. Epub 2005 Apr.
- 9. Schroeder M, Viezens L, Schaefer C, Friedrichs B, Algenstaedt P, Ruther W, Wiesner L, Hansen-Algenstaedt N. Chemokine profile of disc degeneration with acute or chron- ic pain // J Neurosurg Spine. 2013; 18: 496–503.
- 10. Andrade P, Hoogland G, Garcia MA, Steinbusch HW, Daemen MA, Visser-Vandewalle
V. El evated IL-1P and IL-6 levels in lumbar herniated discs in patients with sciatic pain
// Eur Spine J. 2013; 22: 714–20. - 11. Kraychete DC, Sakata RK, Issy AM, Bacellar O, Santos-Jesus R, Carvalho EM. Serum cytokine levels in patients with chronic low back pain due to herniated disc: analyti- cal cross-sectional study // Sao Paulo Med J. 2010; 128 (5): 259–62.
- 12. Watkins LR, Maier SF, Goehler LE. Immune activation: the role of proinflammatory cytokines in inflammation, illness responses and pathological pain states // Pain. 1995; 63 (3): 289–302.
- 13. Nygaard OP, Mellgren SI, Osterud B. The inflammatory properties of contained and non-contained lumbar disc herniation // Spine (Phila Pa 1976). 1997; 22 (21): 2484–88.
- 14. Yoshida M, Nakamura T, Sei A, Kikuchi T, Takagi K, Matsukawa A. Intervertebral disc cells produce tumor necrosis factor alpha, interleukin-1beta and monocyte chemoat- tractant protein-1 immediately after herniation: an experimental study using a new her- nia model // Spine (Phila Pa 1976). 2005; 30 (1): 55–61.
- 15. Koch A, Zacharowski K, Boehm O, Stevens M, Lipfert P, von Giesen HJ, Wolf A, Freynhagen R. Nitric oxide and pro-inflammatory cytokines correlate with pain inten- sity in chronic pain patients // Inflamm Res. 2007; 56 (1): 32–37.
- 16. Monfort J., Nacher M., Montell E. et al. Chondroitin sulfate and Hyaluronic acid (500–730 kDa) inhibit stromelysin-1 synthesis in human osteoarthritic chondrocytes // Drugs Exp Clin Res. 2005. 31: 717–6.
- 17. Chou M.M., Vergnolle N., McDougall J.J. et al. Effects of chondroitin and glu- cosamine sulfate in a dietary bar formulation on inflammation, interleukin-1-beta, matrix metalloprotease-9, and cartilage damage in arthritis // ExpBiol Med. 2005; 230: 255–62.
- 18. Holzmann J., Brandl N., Zemann A. et al. Assorted effects of TGF-beta and chon- droitin sulfate on p38 and ERK1/2 activation levels in human articular chondrocytes stim- ulated with LPS // Osteoarthritis Cartilage. 2006; 14: 519–25.
- 19. Verbruggen G., Veys E.M. Influence of sulphated glycosaminoglycans upon proteo- glycan metabolism of the synovial lining cells // Acta Rhumatol Belg 1977; 1: 75–92.
- 20. Lippielo L., Grande D. In vivo chondroprotection of glucosamine and chondroitin Sul- fate in a rabbit model of a OA and demonstration of metabolic synergy on chondro- cyte in vitro // Ann Rheum. Dis. 2000; 59 (suppl. I): 266.
- 21. Chan P.S., Caron J.P., Orth M.W. Shot-term gene expression changes in cartilage explants stimulated with interleukin beta glusglucosamine and chondroitin sulfate // J rheumatol. 2006; 33: 1329–40.
- 22. Ronca F., Palmieri L., Panicucci P., Ronca G. Anti-inflammatory activity of chon- droitin sulfate // Osteoarthritis Cartilage. 1998; 6: 14–21.
- 23. Алексеева Л.И., Аникин С.Г., Зайцева Е.М. и др. Исследование эффективности, переносимости и безопасности препарата хондрогард у пациентов с остеоартрозом
// Фарматека. — 2013. — № 7. — С. 60–64. - 24. Открытое неконтролируемое исследование эффективности и безопасности парентеральной формы хондроитина сульфата (Мукосат®). Кафедра ревматологии ЛенГИДУВа им. С.М. Кирова, 1990 г. Материалы предоставлены компанией «ДИАМЕД–фарма».
- 25. Инструкция по медицинскому применению препарата Мукосат® PN 000570/01.
- 26. Singh JA, Noorbaloochi S, MacDonald R, Maxwell LJ. Chondroitin for osteoarthritis
// Cochrane Database of Systematic Reviews. 2015, Issue 1. Art. No.: CD005614. - 27. Предоставленные компанией «ДИАМЕД-фарма» материалы ПОБЛ препарата Мукосат® за отчетный период 27 июля 2015 г. — 30 мая 2017 г.
- 28. Hochberg M. C. et al. Combined chondroitin sulfate and glucosamine for painful knee osteoarthritis: a multicentre, randomised, double-blind, non-inferiority trial versus cele- coxib // Annals of the Rheumatic Diseases. 2015; 0: 1–8.
- 29. Martel-Pelletier J., Roubille C., Abram F., Hochberg M. C., Dorais M., Delorme P., Ray- nauld J.-P., Pelletier J.-P. First-line analysis of the effects of treatment on progres- sion of structural changes in knee osteoarthritis over 24 months: data from the osteoarthritis initiative progression cohort // Annals of the Rheumatic Diseases. 2013; 0: 1–10.
- 30. Henrotin Y., Lambert С. Chondroitin and Glucosamine in the Management of Osteoarthri- tis: An Update // Current Rheumatology Reports. 2013; 15: 361.
- 31. Henrotin Y., Marty M., Mobasheri A. What is the current status of chondroitin sul- fate and glucosamine for the treatment of knee osteoarthritis? // Maturitas. 2014; 78; 184–87.
- 32. Wim Jvan Blitterswijk Jos CM van de Nes, Paul IJM Wuisman. Glucosamine and chon- droitin sulfate supplementation to treat symptomatic disc degeneration: Biochemical ratio- nale and case report // BMC Complementary and Alternative Medicine. 2003; 3 (1): 2.
- 33. Bruyеre O., Cooper C., Pelletier J-P., Branco J., Brandi M L., Guillemin F., Hochberg M.C., Kanis J A., Kvien T C., Martel-Pelletier J., Rizzoli R., Silverman S., Reginster J-
Y. An algorithm recommendation for the management of knee osteoarthritis in European dinternationally: A report from a task force of the European Society for Clinical and Eco- nomic Aspects of Osteoporosis and Osteoarthritis (ESCEO) // Seminars in Arthritis and Rheumatism. 2014; 44(3): 253–63. - 34. Ireland D. Molecular mechanisms involved in intervertebral disc degeneration and poten- tial new treatment strategies // Bioscience Horizons. 2009; 2 (1): 83–89.
- 35. Castellsague J, Riera-Guardia N, Calingaert B., Varas-Lorenzo C., Fourrier-Reglat A., Nicotra F.,Sturkenboom M., Perez-Gutthann S. Individual NSAIDs and Upper Gastroin- testinal Complications A Systematic Review and Meta-Analysis of Observational Studies (the SOS Project) // Drug Safety. 2012; 35 (12): 1127–46.
- 36. McGettigan P., Henry D. Cardiovascular Risk with Non-Steroidal Anti-Inflammatory Drugs: Systematic Review of Population Based Controlled Observational Studies // PLoS Medi- cine. 2011; 8 (9): e1001098.
- 37. Баранцевич Е.Р. Рациональная терапия дорсалгий // Manage pain. — 2017. — № 2.
- 38. Olariu L, Dumitriu B, Buse E. Rosoiu N. The «In vitro» effect of Alflutop product on same extracellular signaling factors involved in the osteoarthicular pathology inflammation
// Annals Serieson Biological Sciences. 2015; 4 (2): 7–18. - 39. Klein RG, Bjоrn CJ Eek, Conor W O’Neill, Caren Elin, Vert Mooney, Richard R Derby. Bio- chemical injection treatment for discogenic low back pain: a pilot study // The Spine Journal. 2003; 3: 220–26.















